Endosülfan ve okratoksin-A’nın birlikte sıçanlarda toksisitesi: histopatolojik değişiklikleri
Özet
Bu çalışmanın amacı, histopatolojik değişikliklerini göz önüne alarak, endosülfan ve okratoksin-A’nın (OTA) birleşik halde yetişkin erkek sıçanlara olan etkilerini inceleme ve karşılaştırmadır. Yetişkin erkek sıçanları, her gruba 10 tane sıçan gelmek üzere, rastgele 4 gruplara (bireysel uygulama, birleşik ve kontrol grubu) atandı.Birinci yedirme grubunda her birine 4 ppm dozunda OTA yedirildi, ikinci yedirme grubunda oral besleme aracılığıyla 1 kg sert buğdaya 5 mg endosülfan ekleyip kom yağında yedirildi, üçüncü yedirme grubunda endosülfan ve OTA 30 gün boyunca birleşik verildi.Dördüncü grup kontrol grup olduğundan toksinsiz yemek yedirildi.30 günlük uygulama sonrasında %10 tamponlu formalinin içinde histopatolojik araştırma için doku toplandı.Hematoksilin ve eozin boyalı bölmeler, endosülfan yedirilen gruba kıyasla OTA yedirilen grupta daha da ciddi olan böbrek ve karaciğerde değişken bozulma eğilimli ve nekrotik değişiklikler gösterdi.Yalnız, sonuçlar sadece endosülfan veya sadece OTA yedirilen gruplara kıyasla, birleşik yedirilen gruplarda çok daha belirgindi. Güncel bulgular, OTA ve endosülfanların hastalık sebeplerinde daha belirgin rol oynayabilecek biriken etkileri olabileceğini gösterdi
Anahtar Kelimeler:Okratoksin-A,endosülfan,toksisite,histopatoloji,karaciğer, böbrek
Mikotoksinler, mısır gevreği (mısır, buğday, yulaf ve arpa) ve mısır gevreği yan ürünleri gibi, neredeyse tüm tarımsal ürünlerde bulunur.Küf veya fungi neredeyse her mahsulde iklim koşullarına göre değişken miktarlarda bulunur.Küf büyümesini engellemek için yemek ve hayvan yemi ürünlerin doğru saklanması çok önemlidir.Uygunsuz depolama şekilleri ise aşırı mikotoksinkontaminasyonuna neden olabilir, güncel tarımsal olarak yaygın pestisit eğilimi,tüketim için zehirli hale gelen pestisit kontaminasyonuna neden olabilir. Bu kontaminasyonlar, mahsullerin ekonomik değerinin düşmesinin yanı sıra insan sağlığına da ciddi problemler sunabilir.
Endosülfan yenilebilir ve yenilemez mahsullerde kulalnılan, kalıcı, toksik, geniş-spektrumlu organo-klorininsektisi ve akarisidir. Genellikle tarım, bağcılık ve çiçekçilikte kullanılmış ve kalıcı organik kirletici madde olarak kayda alınmıştır. Hindistan’ın Kerala bölgesinde bulunan Kasargod’unPadre köyünde, endosülfanın, kan, yağ, süt, sebzeler, akaju yaprakları, toprak ve suyu kontamine ettiği raporlanmıştır.
Karaciğer, akciğer, merkezi sinir sistemi, genital sistem, pankreas vs. de dâhil olmak üzere, hem insan hem hayvanların organlarında toksik etkileri vardır. Endosülfan, üreme ve gelişimsel bozukluğa neden olan endokrin engelleyici görevi görür: deneysel hayvanlarda bağışıklık bastırması ve kansere de neden olduğu raporlanmıştır.
Okratoksin-A (OTA), Aspergillus ve Pennicillium`un sayısız özellikleri tarafından salgılanan en toksik mikotoksinlerden biridir. OTA’nın dünya çapında kontaminasyonları, gevrek ve fıstık, kümes hayvanı yemleri, hayvan yemleri, yeşil kahve çekirdeği, kakao çekirdekleri, şarap üzümler, kuru üzüm, ve bira da olmak üzere birçok yemeklerde raporlanmıştır. OTA’nın toksik belirtileri nefrotoksisite, teratojenisite, immünotoksisite, karsinojenisite, ve mutajenisite’yi de kapsar. OTA’nın aynı zamanda, insan Balkan Nefropatisi’ne de neden olduğu düşünülüyor. Bu yüzden, böbrek OTA’nın ana hedeflerinden biri olarak düşünülüyor.Hayvan yeminde yaygın olarak bulunması nedeniyle, OTA’ya maruz kalmamak neredeyse imkansızdır.
Dahası, gerçek hayatta organizmalar eş zamanlı birden fazla toksin veya kirleticiye maruz kalır.Araştırma, bu nedenle erkek sıçanların OTA ve Endosülfana birleşik maruz kalma sonrası karaciğer ve böbreklerindeki patolojik değişiklikleri incelemeye adanmıştır.
Materyaller ve metotlar
OTA’nın üretim ve analizi
Aspergillusochraceus NRRL-3174, ilk başta, Amerika Birleşik Devletlerinin Illinois eyaleti, Peoria’da bulunan Tarımsal Kullanışlılık Araştırma Ulusal Merkezinde üretilmişti. Trenk ve iş arkadaşlarının da önerdiği gibi ilk olarak mısır üzerinde üretilmişti. Toksin örneğinin ele geçirme ve temizleme işlemi AOAC metodu tarafından ve OTA çoğaltılması TLC tarayıcısı tarafından yapılmıştı. (CAMAG,İsviçre).
Zehirli yemin hazırlanması
Kültürü alınmış mısır tozunun bazal oranına (mikotoksin varlığının negatif olduğu kanıtlanmış olan temele) OTA eklemesi yapılmıştır, ekleme 1 kg yeme 4 mg OTA gelecek şekilde ayarlanmıştır.Toksin ve karıştırılmış yemden alınan temsili miktar alınmış ve gelecekte düzgün karıştırılmasından emin olunması için çoğaltılmıştır.
Endosülfan dozu
Endosülfan mısır yapında çözülmüştür ve 1 kilogramlık vücut ağırlığına 5 mg gelecek şekilde 30 gün boyunca erkek sıçanlara oral beslenme ile verilmiştir. Kontrol grubuna ise, endosülfan uygulanmış sıçanların aldığı mısır yağı miktarı kadar miktar verilmiştir.
Deneysel plan
Yetişkin erkek Wistar sıçanları (7-8 haftalık yaş ve 180±20 g ağırlık),HingistanVereriner Araştırma Enstitüsünün Laboratuvar Hayvan Kaynaklarından alınmıştır ve gerektiği zamana kadar standart diyette tutulmuş ve suları verilmiştir. 1 haftalık alışma süresi sonrasında, hayvanlar 10’luk 4 adet gruplara ayrılmış ve şöyle uygulamalar geçirmişlerdir; birinci grup 1 kg ağırlığa 4 mg OTA seviyeli yem ile beslenmiştir;ikinci grup hayvanlar oral beslenme yoluyla 1 kg ağırlığa 5 mg endosülfan oranı ile beslenmiştir; üçüncü grup hem OTA (1 kg ağırlığa 4 mg) hem endosülfan (1 kg ağırlığa 5 mg) beslenmiştir ve dördüncü grup mikotoksinsiz bazal bir diyet ile beslenmiştir. Tüm prosedürler ve hayvanların fedaları Hayvan Etik Kurulu Enstitüsü ve Hayvanlarda Deneyleri Yönetim ve Kontrol Komitesinin onayladığı kılavuza uyar şekilde gerçekleştirilmiştir.
Patolojik değişiklikler
Tüm grupların karaciğer ve böbrekleri ortalama patolojik
değişiklikler için taranmıştır.Islak organ ağırlıkları, işlem yapmak için toplanan doku öncesi kayıtlara geçirilmiştir. Histopatolojik çalışmalar için temsili doku örnekleri %10 destekli formalinde alınmıştır. Dokular uygunca işlenmiş ve parafin mumuna yerleştirilmiştir. Bölmeler Hematoksilin ve eosin boyası ile boyanmıştır ve ışık mikroskopu altında incelenmiştir.
İstatistik Analiz
Araştırma sırasında toplanan veriler, gruplar arasındaki araç değişikliklerini belirlemek için öğrencilerin ‘t’ testi kullanılmıştır. Tüm analizler GraphPadInStat (San Diego, ABD) yazılımı ile gerçekleştirilmişti Tüm önemli açıklamalar <0.05’lik bir negatif olasılık oranına dayanılarak yapılmıştır.
Sonuç
Ortalama lezyon ve böbrek ve karaciğerin genel ağırlığı
30 gün boyunca OTA, Endosülfan veya onların birleşmiş hali yedirilen farelerde yapılan makroskobik araştırmalar karaciğer yüzeyinde fokal alanlar gösterdi. Karaciğer az soluk ve deri değiştirmişti Kontrol grubu ile kıyasla, sadece OTA yedirilen birinci grupta ve OTA ve endosülfan yedirilen üçüncü grupta karaciğer ağırlığında azalma görüldü. Düşüş özellikle üçüncü grupta yüksekti..
Okratoksin-A(OTA)uygulama
Böbrek
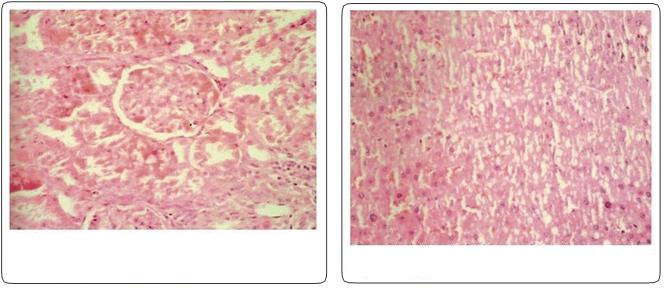
.Kontrol grubuna göre, OTA uygulanan hayvanların yakınsal karışık tübüllerinde dejeneratif değişiklikler ile birlikte lümende pembemsi homojenik kütle bulundu.Bazı tübüller fiknotik ve karyorhektik çekirdekler gösterdi. Vasküler sıkışıklık hem kabukta hem ilikte bulundu.Birkaç glomeruli, bowman alanının proteinli kütle birikimi nedeniyle genişlediğini gösterdi. Tubüler lümenin sıralanan epitel hücrelerin dejenerasyon ve şişme nedeniyle yok olması nedeniyle yok olduğu gözlemlendi.

Figür1.Böbrek bölümü normal gromerüller ve yakın ve uzaksal karışık tübüller gösteriyor.H&E×100.
Tablo1.Yetişkin erkek sıçanlara OTA ve endosülfan uygulama sonrası karaciğer ve böbreğin ortalama ağırlığı.
Grup→ KontrolOTAEndosülfan Birleşik Önem
(ES) (OTA+ES)
|
Organlar |
Organ ağırlığının ortalama alınması±SE (n=10) |
|
|
Karaciğer Böbrek |
3.93±0.24b 3.27±0.66a 3.57±0.18ab 3.12±0.11a 1.03±0.07b 0.79±99a 0.86±0.04b 0.70±0.064 |
P<0.05 P<0.05 |
En azından bir süper simge taşıyan ortalama gruplar arasında çok da fark etmemiştir.


Karaciğer
Toksinsiz beslenen sıçanların karaciğer şemaları düzgündü.(Figür3).InKarşılaştırıldığında, OTA yedirilen sıçanların hepatositleri granüler sitoplazmada dejeneratif ve nekrotik değişiklikler gösterdi.(Figür 4).Çoğu hepatositlerdeki sitoplazma soluk veya daha az lekeliydi. Merkezi ve portal damarlar ile hepatik sinüs eğrileri, az ile orta arasında tıkanma gösterdi Merkezi lob bölümünün hepatositlerinde hafiften ortaya kadar yağ değişiklikleri gözlemlendi. (Figür 4)
Endosülfan uygulaması
Böbrek
İkinci gruptaki yakınsal karışık tübüller, sıralama hücrelerinde dejenerasyon ve nekroz ortaya çıkardı Tubüller lümen, ayrı nekrozlu pembemsi kütlenin varlığını ortaya koydu (Figür 5). .Inter-tubüler damarlar hafifçe tıkanmış görüntülendi.
Karaciğer
Sadece OTA alan grup ile kıyasla, endosülfan alan ikinci gruplardaki hepatositler, granüler sitoplazmada hafif dejenerasyon gösterdi(Figür6).
Endosülfan + OTA birleşik uygulama
Böbrek
Üçüncü grupta, yakınsal karışık tubüller epitel hücrelerin sıralanmasında vaküolasyonlar ve sitoplazmanın pembemsi granüllerinde dejeneratif değişiklikler gösterdi.(Figür7).Hücrelerin şişmesi lümenin tıkanmasına neden oldu. Bazı glomeruli, pembemsi homojenlerin varlığını gösterdi

Karaciğer
Üçüncü grup hayvanlarında hepatik sinusoidler ve portal damarları hafif ve orta derece arası tıkanma gösterdi.Hepatositlerde sitoplazmadaki ince granüllerde şişme ve bazen iki çekirdek gözlemlendi. Hepatik lobüllerdejenerasyon ve küçükten büyüğe yağ kofullarının varlığının, çekirdeği perifere ittiğini gösterdi.(Figür 8). Thesefatty Bu yağ değişiklikleri genellikle merkezi damar etrafında gözlemlendi. Bazı yerlerde portal lobüllerin merkezinde, portal üçlüsünün etrafında mononükleer hücre tepkileri gözlemlendi.
Nekrozlu fokal alanlarda, izole hepatositler hepatik özel dokunun birkaç yerinde gözlemlendi. (Figür 8).
Tartışma
Ortalama gözlenen lezyonlar şişmiş ve biraz benekli karaciğer ve biraz soluk böbreklerdi.Bu organların da genel ağırlıklarının azalmış olduğu gözlemlendi. Karaciğer ve böbrekteki bu değişiklikler, birleşik OTA ve Endosülfan grubunda, tekli gruplara göre daha baskındı Bu gözlemler daha önce fark edilen bulgular ile eşleşmektedir.
Karaciğer ve böbreklerin kesin ortalama organ ağırlığı, endosülfan verilmiş sıçanlarda ve civcivlerde aynıydı. Bizim organ ağırlığı hakkında yaptığımız gözlemlemelere karşın, karaciğer ve böbrekte daha önce yapılan çalışmalar bir büyüme gözlemlemiştir. Bu değişiklikler yaş, cinsiyet ve hayvanlardaki baskı, aracın veya uygulama rejimeni değişikliği gibi birçok değişik faktörlerden kaynaklanabilir.OTA ve Endosülfan kendi başlarına karaciğer ve böbrekte solgunlaşma ve histopatolojik incelemede görünen dejeneratif etkilere atanabilecek karaciğer hassaslaşmasına neden olur.OTA ve Endosülfan hepatotoksik ve nefratoksik olarak bilinir.Bu efektler bizim deneysel sıçanımızda görüntülenmiştir.Karaciğerdeki değişiklikler doğasında dejeneratifti, örneğin yağ değişiklikleri ve vasküler tıkanma.Benzer değişiklikler daha önce çalışma yapanlar tarafından da başka hayvanlarda bulunmuştur, mesela sıçan, tavşanlar ve kümes hayvanları.Böbrek tübüllerinde ve böbrek kan hücrelerinde bulunan dejeneratif ve vasküler değişiklikler, daha önceki bulgular ile örtüşmektedir.OTA veya Endosülfan dozajlarının düşüklüğü nedeniyle güncel çalışmada bulunan ortalama veya mikroskobik sonuçlar hafif olarak sınıflandırılabilir.Böbreklerdeki histopatolojik değişiklikler, bir bölümünü de olsa, bu deneysel sıçanların bir önceki incelemede kaydedilen serum analizlerindeki fonksiyonel değişikliklerini açıklamasına yardımcı olur.Güncel araştırmadan OTA ve Endosülfanın böbrek ve karaciğere birleşik halde tek halde olduğundan daha çok toksik olduğu sonucuna varılmıştır.
Competinginterests
Theauthorsdeclarethattheyhavenocompetinginterests.
Authors’contributions
|
Authors’contributions |
SNK |
BB |
AGT |
KPS |
RS |
AKJ |
|
Researchconceptanddesign |
✓ |
-- |
✓ |
-- |
✓ |
-- |
|
Collectionand/orassemblyofdata |
✓ |
-- |
-- |
✓ |
-- |
-- |
|
Dataanalysisandinterpretation |
✓ |
-- |
-- |
✓ |
-- |
-- |
|
Writingthearticle |
✓ |
✓ |
-- |
-- |
-- |
✓ |
|
Criticalrevisionofthearticle |
-- |
-- |
-- |
-- |
-- |
✓ |
|
Finalapprovalofarticle |
-- |
-- |
-- |
-- |
-- |
✓ |
|
Statisticalanalysis |
-- |
-- |
✓ |
✓ |
-- |
✓ |
Acknowledgement
Theresearcherswouldliketoacknowledgethehelpextended
byIn-charge,DivisionofPathology,IndianVeterinary
ResearchInstitute.
Publicationhistory
Editor:LingyanWang,OregonHealth&ScienceUniversity,Portland.
EIC:GaetanoGiuseppeMagro,UniversityofCatania,Italy. Received:29-Sep-2015FinalRevised:03-Nov-2015
Accepted:13-Nov-2015Published:23-Nov-2015
References
- Du H, Wang M, Dai H, Hong W, Wang J, Weng N, Nie Y and Xu A. Endosulfan isomers and sulfate metabolite induced reproductive toxicity in Caenorhabditis elegans involves genotoxic response genes. Environ Sci Technol. 2015; 49:2460-8. | Article | PubMed
- Omnipresent Poison. | Website
- Ramesh A and Vijayalakshmi A. Environmental exposure to residues after aerial spraying of endosulfan: residues in cow milk, fish, water, soil and cashew leaf in Kasargode, Kerala, India. Pest Manag Sci. 2002; 58:1048-54. | Article | PubMed
- O. Ozmen. Pathology of Endosulfan. in Pesticides in the Modern World - Effects of Pesticides Exposure, M. Stoytcheva, Ed. InTech. 2011.
- Gupta PK and Gupta RC. Pharmacology, toxicology and degradation of endosulfan A review. Toxicology. 1979; 13:115-30. | Article | PubMed
- Sutherland TD, Home I, Weir KM, Russell RJ and Oakeshott JG. Toxicity and residues of endosulfan isomers. Rev Environ Contam Toxicol. 2004; 183:99-113. | Article | PubMed
- N. D. Singh, A. K. Sharma, P. Dwivedi, Kumar M and R. D. Patil. Immunosuppressive effect of combined citrinin and endosulfan toxicity in pregnant Wistar rats. Vet. Arh. 2011; 81. | Article
- Singh ND, Sharma AK, Dwivedi P, Patil RD and Kumar M. Citrinin and endosulfan induced teratogenic effects in Wistar rats. J Appl Toxicol. 2007; 27:143-51. | Article | PubMed
- Singh ND, Sharma AK, Dwivedi P, Patil RD and Kumar M. Citrinin and endosulfan induced maternal toxicity in pregnant Wistar rats: pathomorphological study. J Appl Toxicol. 2007; 27:589-601. | Article | PubMed
- S. N. Kumar A. G. Telang R. D. Patil A. K. Jain and K. P. Singh. Cytogenetic Effects of Combined Ochratoxin A and Endosulfan in Rats. J. Environ. Anal. Toxicol. 2014; 4:1. | Article
- Baudrimont I, Sostaric B, Yenot C, Betbeder AM, Dano-Djedje S, Sanni A, Steyn PS and Creppy EE. Aspartame prevents the karyomegaly induced by ochratoxin A in rat kidney. Arch Toxicol. 2001; 75:176-83. | Article | PubMed
- Al-Anati L and Petzinger E. Immunotoxic activity of ochratoxin A. J Vet Pharmacol Ther. 2006; 29:79-90. | Article | PubMed
- Magnoli C, Hallak C, Astoreca A, Ponsone L, Chiacchiera S and Dalcero AM. Occurrence of ochratoxin A-producing fungi in commercial corn kernels in Argentina. Mycopathologia. 2006; 161:53-8. | Article | PubMed
- Rosa CA, Ribeiro JM, Fraga MJ, Gatti M, Cavaglieri LR, Magnoli CE, Dalcero AM and Lopes CW. Mycoflora of poultry feeds and ochratoxin-producing ability of isolated Aspergillus and Penicillium species. Vet Microbiol. 2006; 113:89-96. | Article | PubMed
- Magnoli C, Hallak C, Astoreca A, Ponsone L, Chiacchiera SM, Palacio G and Dalcero A. Surveillance of toxigenic fungi and ochratoxin A in feedstuffs from Cordoba Province, Argentina. Vet Res Commun. 2005; 29:431-45. | Article | PubMed
- Romani S, Sacchetti G, Chaves Lopez C, Pinnavaia GG and Dalla Rosa M. Screening on the occurrence of ochratoxin A in green coffee beans of different origins and types. J Agric Food Chem. 2000; 48:3616-9. | Article | PubMed
- Serra Bonvehi J. Occurrence of ochratoxin A in cocoa products and chocolate. J Agric Food Chem. 2004; 52:6347-52. | Article | PubMed
- Magnoli C, Violante M, Combina M, Palacio G and Dalcero A. Mycoflora and ochratoxin-producing strains of Aspergillus section Nigri in wine grapes in Argentina. Lett Appl Microbiol. 2003; 37:179-84. | Article | PubMed
- Magnoli C, Astoreca A, Ponsone L, Combina M, Palacio G, Rosa CA and Dalcero AM. Survey of mycoflora and ochratoxin A in dried vine fruits from Argentina markets. Lett Appl Microbiol. 2004; 39:326-31. | Article | PubMed
- Medina A, Jimenez M, Gimeno-Adelantado JV, Valle-Algarra FM and Mateo R. Determination of ochratoxin A in beer marketed in Spain by liquid chromatography with fluorescence detection using lead hydroxyacetate as a clean-up agent. J Chromatogr A. 2005; 1083:7-13. | Article | PubMed
- Pfohl-Leszkowicz A and Manderville RA. Ochratoxin A: An overview on toxicity and carcinogenicity in animals and humans. Mol Nutr Food Res. 2007; 51:61-99. | Article | PubMed
- Gekle M, Schwerdt G, Freudinger R, Mildenberger S, Wilflingseder D, Pollack V, Dander M and Schramek H. Ochratoxin A induces JNK activation and apoptosis in MDCK-C7 cells at nanomolar concentrations. J Pharmacol Exp Ther. 2000; 293:837-44. | Article | PubMed
- Liang R, Shen XL, Zhang B, Li Y, Xu W, Zhao C, Luo Y and Huang K. Apoptosis signal-regulating kinase 1 promotes Ochratoxin A-induced renal cytotoxicity. Sci Rep. 2015; 5:8078. | Article | PubMed
- Kuiper-Goodman T and Scott PM. Risk assessment of the mycotoxin ochratoxin A. Biomed Environ Sci. 1989; 2:179-248. | Article | PubMed
- Simon P, Godin M and Fillastre JP. Ochratoxin a: a new environmental factor which is toxic for the kidney? Nephrol Dial Transplant. 1996; 11:2389-91. | Article | PubMed
- Trenk HL, Butz ME and Chu FS. Production of ochratoxins in different cereal products by Aspergillus ochraceus. Appl Microbiol. 1971; 21:1032-5. | PubMed Abstract | PubMed Full Text
- P. Cunniff and Association of Official Analytical Chemists. Official methods of analysis of the AOAC International. Washington (D.C.): AOAC International. 1995.
- L. G. Luna. Manual of histologic staining methods of the Armed Forces Institute of Pathology. 1968.
- Choudhary N, Sharma M, Verma P and Joshi SC. Hepato and nephrotoxicity in rat exposed to endosulfan. J Environ Biol. 2003; 24:305-8. | Article | PubMed
- K. Prasanna, A. K. Sharma, P. Dwivedi, C. C. Satheesh and A. G. Telang. Pathogenesis of ochratoxin A induced nephropathy in rats with special reference to oxidative damage, cytokine profile and ultrastructural changes. Indian J. Vet. Pathol. 2007; 31:1–10. | Article
- Wangikar PB, Dwivedi P, Sharma AK and Sinha N. Effect in rats of simultaneous prenatal exposure to ochratoxin A and aflatoxin B1. II. Histopathological features of teratological anomalies induced in fetuses. Birth Defects Res B Dev Reprod Toxicol. 2004; 71:352-8. | Article | PubMed
- Dortant PM, Peters-Volleberg GW, Van Loveren H, Marquardt RR and Speijers GJ. Age-related differences in the toxicity of ochratoxin A in female rats. Food Chem Toxicol. 2001; 39:55-65. | Article | PubMed
- N. V. Kurkure, A. G. Bhandarkar, M. V. Joshi, R. D. Sadekar and S. S. Bhagwat. Immunosuppressive and histotoxic effects of endosulphan in chicks. Indian J. Anim. Sci. India. 1993.
- Munro IC, Moodie CA, Kuiper-Goodman T, Scott PM and Grice HC. Toxicologic changes in rats fed graded dietary levels of ochratoxin A. Toxicol Appl Pharmacol. 1974; 28:180-8. | Article | PubMed
- Kiran R and Varma MN. Biochemical studies on endosulfan toxicity in different age groups of rats. Toxicol Lett. 1988; 44:247-52. | Article | PubMed
- C. C. Satheesh, A. K. Sharma, K. Prasanna and P. Dwivedi. Ultrastructural changes in kidneys and liver in experimentally induced ochratoxicosis in wister rats. Indian J. Vet. Pathol. India. 2004. | Article
- M. S. Mir, P. Dwivedi and K. Charan. Ochratoxin A induced acute toxicity in rabbits. 1999.
- M. S. Mir and P. Dwivedi. Clinical studies on experimental subacute ochratoxicosis in rabbits. Indian J Vet Pathol. 2000; 24:99-101.
- Wangikar PB, Dwivedi P, Sinha N, Sharma AK and Telang AG. Teratogenic effects in rabbits of simultaneous exposure to ochratoxin A and aflatoxin B1 with special reference to microscopic effects. Toxicology. 2005; 215:37-47. | Article | PubMed
- Dwivedi P, Burns RB and Maxwell MH. Ultrastructural study of the liver and kidney in ochratoxicosis A in young broiler chicks. Res Vet Sci. 1984; 36:104-16. | Article | PubMed
- Hack R, Ebert E and Leist KH. Chronic toxicity and carcinogenicity studies with the insecticide endosulfan in rats and mice. Food Chem Toxicol. 1995; 33:941-50. | Article | PubMed
- S. N. Kumar, A. G. Telang, K. P. Singh, B. Bastia and A. K. Jain. Toxic Manifestation of Endosulfan and Ochratoxin- A in Adult Male Rats. MOJ Toxicol. 2015; 1:00012. | Pdf
Combined toxicity of endosulfan and ochratoxin-A in rats: histopathological changes
Shashi Nandar Kumar1, Banajit Bastia1, Avinash Gopal Telang2, Karam Pal Singh2, Rambir Singh3 and Arun Kumar Jain1*
*Correspondence: Arun Kumar Jain [email protected]
1. Environmental Toxicology Lab, National Institute of Pathology (ICMR), Safdarjung Hospital Campus, New Delhi-110029, India.
Çeviren ve Derleyen ; Ayşegül Kazan
Kaynak:<http://www.hoajonline.com/histology/2055-091X/2/22>
Histoloji
-
Endosülfan ve okratoksin-A’nın birlikte sıçanlarda toksisitesi: histopatolojik değişiklikleri
-
Histoloji Pdf Ders Notları
-
DEKALSİFİYE EDİLMEMİŞ KESİTLERİN HAZIRLANIŞI
-
DEKALSİFİKASYONU TEST ETMEK
-
KELATLAMA AJANLARI
-
ELEKTROLİTİK DEKALSİFİKASYON
-
ASİT DEKALSİFİKASYON SIVILARI
-
Histopatoloji nedir ?
-
KEMİK DOKUSU VE DEKALSİFİKASYON
-
MSS’DE DEJENERE MİYELİNİN GÖSTERİMİ
-
MARKSCHE’DEN BOYASI (Spielmayer, Benda)
-
MSS‘DE MİYELİNİN GÖSTERİMİ
-
KARIŞIK OLAN TEKNİK
-
BİELSCHOWSKY TEKNİĞİ
-
GÜMÜŞ ÇÖKTÜRME YÖNTEMLERİ